Hola estimados amigos!
Empecemos definiendo un ion común, como aquel ion que es proporcionado por más de dos especies en la misma solución.
Ahora bien, en algunas ocasiones es necesario separar un ion de una solución, para determinar su concentración, sin embargo siempre quedarán algunos iones disueltos. A nivel experimental se puede adicionar una sal que provea un ion común para variar la solubilidad y lograr una mayor separación.
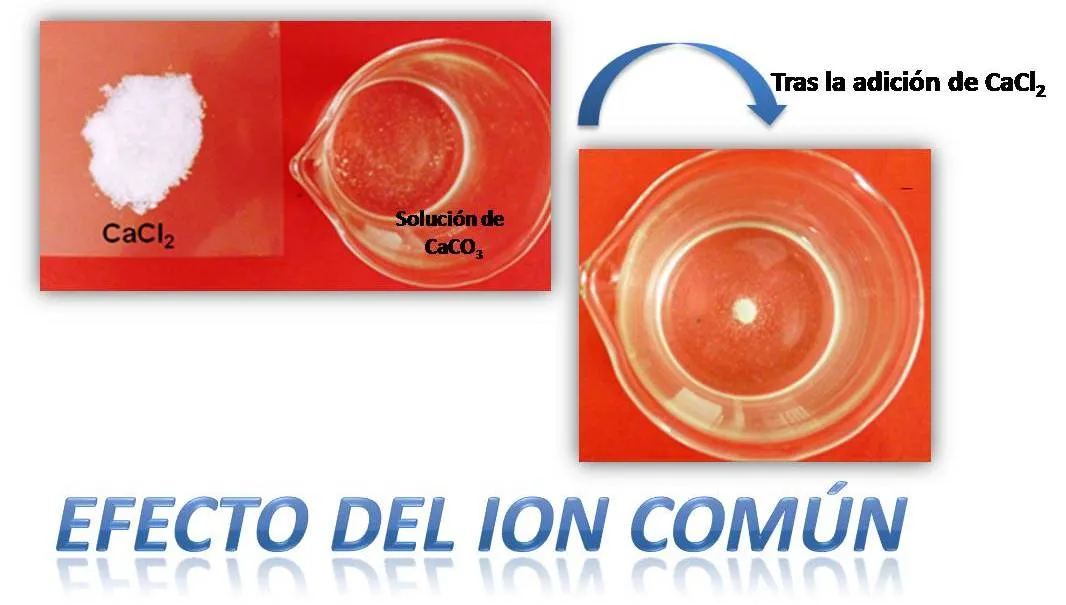
Fuente:@yusvelasquez
¡Veamos cual es su efecto!
Analicemos desde el punto de vista cualitativo
Por ejemplo, si disolvemos carbonato de sodio en agua, y posteriormente se le adiciona una sal como el cloruro de calcio, observaremos como parte de los iones disueltos regresan a su fase original sólida. Esto se puede explicar basado en el Principio de Le Chatelier, el cual establece que al añadir una sal que provea un ion común, el equilibrio se perderá y buscará la manera de ajustarse nuevamente, y esto en este caso se logra disminuyendo la concentración de los iones añadidos por lo que la reacción se desplazará de derecha a izquierda disminuyendo así la solubilidad de la sal y produciendo su precipitación obteniendo mayor cantidad de masa del analito en estudio.
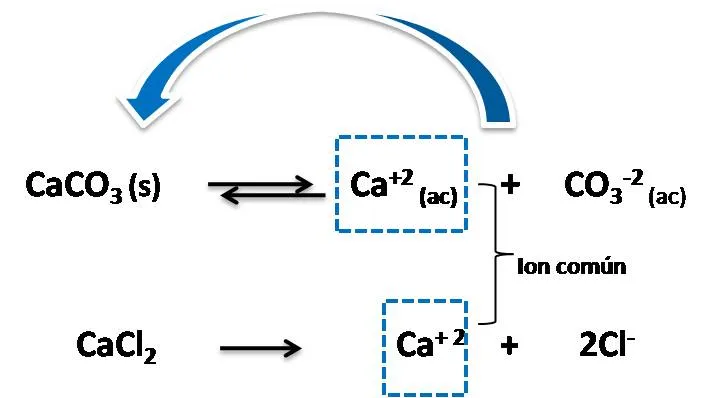
Fuente:@yusvelasquez
En este caso se puede observar como ambas sales proveen iones Ca+2, esto ocasiona que el producto iónico (Qps) aumente, y supere el valor de Kps, lo cual también indica que se tiene una solución sobresaturada y para alcanzar el equilibrio precipitará mayor cantidad de carbonato hasta que los dos valores se igualen.
Un aspecto también importante, es que en caso de que se requiera disolver el precipitado, se procedería de manera contraria, removiendo un ion, lo cual incrementaría la solubilidad de la sal, sin embargo ya no se trataría de un ion común. Por ejemplo, los precipitados de carbonatos al adicionarles ácido se pueden disolver, esto debido a que los iones CO3-2 reaccionan con el ácido desplazando la reacción de izquierda a derecha aumentando así la solubilidad. Este fundamento es lo que explica lo que sucede cuando la lluvia ácida ocasiona daños a construcciones, monumentos de mármol, o piedra caliza.
Desde el punto de vista cuantitativo
Estudiar numéricamente el efecto del ion común resulta un poco difícil, ya que en solución los iones interactúan constantemente con otros iones presentes, sin embargo mediante el empleo del Kps de la sal poco soluble se puede obtener una idea de su influencia.
Sigamos con el ejemplo anterior y calculemos en primer lugar la solubilidad del carbonato de calcio en agua. Para ello emplearemos el valor de Kps obtenido de la bibliografía.
Parte 1. Solubilidad del carbonato de calcio en agua
- Partimos de la reacción de disociación de la sal
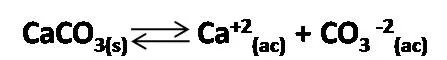
- Expresamos la constante del producto de solubilidad (Kps)
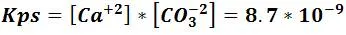
- Calculemos la solubilidad (S ) partiendo del valor del Kps
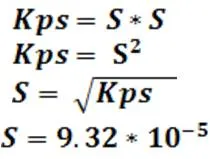
Parte 2. Solubilidad del carbonato de calcio al adicionar un ion común
Calculemos la solubilidad al adicionar una solución 0.10 mol/L de CaCl2 y comparemos los resultados.
- Partimos de las reacciones involucradas
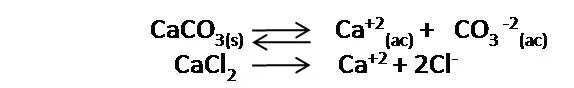
- Expresamos la constante del producto de solubilidad (Kps)
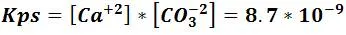
Calculemos la solubilidad partiendo del valor del Kps y tomando en cuenta el aporte en la concentración del ion calcio por la adición del cloruro.
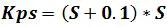
Se sustituyen los valores en la ecuación y al resolver se obtiene
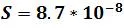
Como se puede observar en la primera parte se obtuvo un valor de solubilidad igual a 9.32x10-5 mientras que al adicionar una sal que provee un ion común la solubilidad disminuyó a 8.7x10-8 confirmando así lo establecido por el Principio de Le Chatelier.
Aplicaciones
Tanto en el laboratorio para análisis de muestras y mediciones cuantitativas como a nivel industrial en diversos procesos tiene su aplicación. Por ejemplo, en la elaboración de jabones, la cual se obtiene mediante una reacción de saponificación, donde reacciona la grasa con hidróxido de sodio se adiciona cloruro de sodio en una etapa conocida como salado con la finalidad de lograr la mayor separación del jabón de la glicerina aumentando así el rendimiento. Por otro parte, para la disminución de la dureza en agua cruda o ablandamiento se le adiciona carbonato de sodio y cal para lograr su precipitación como carbonatos o hidróxidos.
Como vemos resulta importante analizar el efecto que ocasiona la adición de un ion común en la solubilidad de las sales poco solubles, de manera que se puedan realizar las diferentes variaciones para lograr el desplazamiento del equilibrio para lograr una mayor separación del compuesto.
¡Espero el contenido sea de su utilidad, hasta una próxima oportunidad, gracias por leer!
Referencias
- Atkins, P. y Jones, L. (2006). Principios de Química. Los caminos del descubrimiento. Buenos Aires: Médica Panamericana.
- Ion común. Disponible en: wikipedia.com
- Jabón. Disponible en: wikipedia.com
